Schweizer Forschende lüften Quantengeheimnisse des Wassers
Forschende aus Lausanne messen erstmals Quanteneffekte bei H-Brücken direkt und ermöglichen neue Einblicke in molekulare Prozesse.

Ein Team der EPFL hat durch Spektroskopie erstmals Quanteneffekte bei Wasserstoffbrückenbindungen in flüssigem Wasser direkt gemessen.
Foto: PantherMedia / Dvorak (YAYMicro)
Wasser ist die Grundlage allen Lebens, und seine besondere molekulare Struktur sorgt für einzigartige Eigenschaften. Doch die genauen Mechanismen, die Wasserstoffbrückenbindungen (H-Brücken) formen, blieben bisher weitgehend ein Rätsel. Forschende der École Polytechnique Fédérale de Lausanne (EPFL) haben nun erstmals ausschließlich Moleküle beobachtet, die an diesen Wasserstoffbrückenbindungen beteiligt sind, und konnten dabei elektronische und nukleare Quanteneffekte direkt messen. Diese Ergebnisse waren bisher nur durch theoretische Simulationen zugänglich.
„Diese Ladungsaufteilung ist ein wesentliches Merkmal des dreidimensionalen H-Bindungsnetzwerks, das flüssigem Wasser seine einzigartigen Eigenschaften verleiht“, so die Forschungsleiterin Sylvie Roke. Die neu entwickelte Technik könnte auf alle Arten von Flüssigkeiten und Lösungen angewandt werden und so tiefere Einblicke in molekulare Strukturen liefern.
Inhaltsverzeichnis
Die Rolle der Wasserstoffbrückenbindungen
Wasserstoffbrückenbindungen entstehen, wenn Wasserstoff- und Sauerstoffatome zwischen Wassermolekülen interagieren. Diese Bindungen, bei denen die Moleküle elektronische Ladung teilen, spielen eine zentrale Rolle im dreidimensionalen Netzwerk, das die Struktur und Eigenschaften von Wasser prägt. Solche Wechselwirkungen verleihen Wasser die Fähigkeit, Wärme zu speichern und Oberflächenspannung zu bilden, sowie seine herausragende Lösungseigenschaft.
Dennoch blieben die quantenmechanischen Aspekte dieser Bindungen bislang theoretische Annahmen. Erst durch den Einsatz der neuen Methode namens korrelierte Schwingungsspektroskopie (CVS) gelang es dem EPFL-Team, die komplexen Quanteneffekte dieser Bindungen im flüssigen Wasser experimentell nachzuweisen.
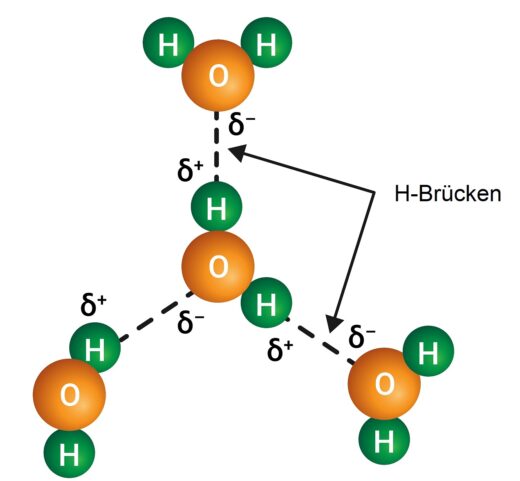
Die Wasserstoffbrückenbindung zwischen zwei Wassermolekülen – die eigentlichen H-Brücken sind gestrichelt eingezeichnet.
Foto: PantherMedia / samjore
So funktioniert die CVS-Technik
Unter der Leitung von Sylvie Roke entwickelte das Team die CVS-Technik, die es ermöglicht, zwischen H-gebundenen und nicht-gebundenen Wassermolekülen zu unterscheiden. Im Gegensatz zu bisherigen Methoden, bei denen alle Moleküle im Wasser gemeinsam analysiert werden, erlaubt CVS gezielte Messungen der Bindungen. Dies stellt einen Durchbruch dar, da es bisher nicht möglich war, zwischen den unterschiedlichen Arten von Molekülwechselwirkungen zu unterscheiden.
„Bei den derzeitigen Spektroskopiemethoden wird die Streuung von Laserlicht gemessen, die durch die Schwingungen aller Moleküle in einem System verursacht wird“, erläutert Roke. „Man muss also raten oder davon ausgehen, dass das, was man sieht, auf die molekulare Interaktion zurückzuführen ist, die einen interessiert.“ CVS hingegen bietet präzisere Informationen über die Ladungsaufteilung und die Stärke der Bindungen.
Einzigartige Erkenntnisse über die Quanteneffekte im Wasser
Um die Unterschiede zwischen H-gebundenen und nicht-gebundenen Molekülen zu messen, nutzten die Forschenden ultrakurze Femtosekunden-Laserpulse im nahen Infrarotbereich. Diese Pulse, die nur eine Billiardstel Sekunde dauern, erzeugen winzige Ladungsschwingungen und atomare Verschiebungen. Daraus resultiert die Emission von sichtbarem Licht, das detaillierte Informationen über die molekulare Struktur und die Ladungsverschiebungen innerhalb und zwischen den Molekülen liefert.
Ein spektrographischer Detektor, der üblicherweise in einem 90-Grad-Winkel zum Laserstrahl positioniert wird, konnte bei CVS auch aus anderen Winkeln genutzt werden, um zusätzliche Informationen über die Molekülanordnung zu gewinnen. Die unterschiedlichen Positionen des Detektors ermöglichten es, spezifische Spektren für H-gebundene und nicht-H-gebundene Moleküle zu erzeugen. Dies eröffnet neue Möglichkeiten zur Analyse der molekularen Dynamik.
Einfluss von pH-Wert-Änderungen auf die H-Bindungen
Das Forschungsteam untersuchte zudem, wie sich Änderungen des pH-Werts auf die Wasserstoffbrückenbindungen auswirken. Sie fügten dem Wasser entweder Hydroxidionen (für basische Bedingungen) oder Protonen (für saure Bedingungen) hinzu. „Hydroxidionen und Protonen sind an der Wasserstoffbrückenbindung beteiligt, sodass eine Änderung des pH-Werts von Wasser dessen Reaktivität verändert“, erklärt der Doktorand Mischa Flór, Erstautor der Studie.
Mit CVS konnten die Forschenden präzise messen, wie viel Ladung Hydroxidionen (8 %) an die Wasserstoffbrückenbindungen abgeben und wie viel Protonen (4 %) aufnehmen. Diese detaillierten Daten wurden durch Simulationen erklärt, die in Zusammenarbeit mit Forschungspartnern aus Frankreich, Italien und Großbritannien erstellt wurden.
Ein breites Anwendungsfeld für CVS
Die Forschenden betonen, dass CVS nicht auf Wasser beschränkt ist, sondern auf eine Vielzahl anderer Flüssigkeiten und Materialien angewandt werden kann. Die Technologie verspricht tiefere Einblicke in chemische Prozesse in Lösungen und Systemen, die Elektrolyte, Aminosäuren, DNA oder Proteine enthalten.
„Die Möglichkeit, die Stärke von Wasserstoffbrückenbindungen direkt zu quantifizieren, ist eine leistungsstarke Methode, mit der sich Details auf molekularer Ebene jeder Lösung klären lassen,“ sagt Roke. CVS bietet also ein vielversprechendes Potenzial zur Untersuchung von Wechselwirkungen in der Materialwissenschaft, der Biochemie und der Umweltforschung.
Ein Beitrag von:


















