Arzneistoffe in Nanopartikeln: Per Anhalter durch den Körper
MIT-Forscher haben eine Strategie entwickelt, um Pharmaka an die richtige Stelle im Gelenk zu transportieren. Sie arbeiten mit Nanopartikeln aus Dendrimeren, also stark verzweigten Molekülen.
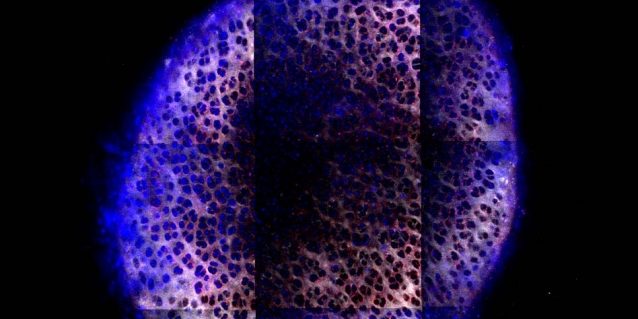
6 Tage nach der Behandlung mit dem Medikament IGF-1, das von Dendrimer-Nanopartikeln (blau gefärbt) getragen wird, haben die Partikel den Knorpel des Kniegelenks durchdrungen.
Foto: MIT/Brett Geiger, Jeff Wyckoff
Mittlerweile gibt es eine Reihe hochwirksamer Moleküle, um etliche Erkrankungen zu therapieren. In der Praxis treten jedoch 2 entscheidende Probleme auf. Manche Pharmaka erreichen das erkrankte Gewebe nicht. Das können Knorpelschichten beim Gelenkverschleiß, der Arthritis, sein. Chemotherapeutika wirken bei Krebs oft recht unspezifisch. Sie schädigen auch gesundes Gewebe. MIT-Forscher zeigen jetzt, welches Potenzial in Nanopartikeln aus Dendrimeren steckt. Wirkstoffe bleiben länger aktiv und gelange in tiefere Gewebsschichten.
Neuer Wirkstoff enttäuscht in Studien
Auch hierzulande leiden Millionen von Menschen am Gelenkverschleiß aufgrund einer fortschreitenden Zerstörung von Knorpelgewebe. Der experimentelle Wirkstoff Insulin-like growth factor 1 (IGF-1), ein Protein, schnitt in Tierexperimenten gut ab, scheiterte jedoch in klinischen Studien. Möglicherweise wird IGF-1 abgebaut, bevor es seinen eigentlichen Wirkort erreicht.
Baumartige Strukturen entstehen
Doch MIT-Wissenschaftler hatten eine Idee. Sie synthetisierten ausgehend von IGF-1 verzweigte Molekülstrukturen, deren Verästelungen an einen Baum erinnern, Chemiker sprechen von Dendrimeren. Ihre neuen Moleküle tragen an der Spitze jedes „Zweigs“ eine positive Ladung. IGF-1 allein liegt in einer zwitterionischen Struktur vor, das heißt positive und negative Ladungen halten sich die Waage. Nach außen ist das Molekül ungeladen. Beim Dendrimer kam auch Polyethylenglykol (PEG) zum Einsatz. Das wasserlösliche Polymer wird in der Pharmazie seit Jahren angewendet. Es ist nicht toxisch, wasserlöslich und durchdringt biologische Barrieren gut.
Erfolgreich im Tierexperiment
Als die Forscher ihre Dendrimere in die Kniegelenke von Ratten injizierten, fanden sie heraus, dass die biologische Halbwertszeit bei 4 Tagen liegt. Das ist 10 Mal mehr als bei reinem IGF-1. Die Medikamentenkonzentration im Gelenk war für 30 Tage hoch genug, um eine Wirkung zu erzielen. IGF-1 fördert das Zellwachstum und verhindert den Zelltod. Unter der Dendrimer-Therapie wurden die Gelenke weitaus geringer geschädigt als bei der Gabe von reinem IGF-1. Das bedeutet auch: Arzneistoffe müssten seltener verabreicht werden und wirken durch die Nanopartikel länger.
Leichter Transport in tiefe Schichten
Wie das funktioniert, erklärt MIT-Forscher Brett Geiger so: Wenn Partikel in ein Gelenk injiziert werden, erreichen sie zuerst die Oberfläche von Knorpeln. Aufgrund ihrer positiven Ladungen haften sie gut an den Strukturen und werden nicht so leicht von der Gelenksflüssigkeit weggespült. Dank der PEG-Ketten diffundieren die Moleküle anschließend in tiefere Schichten. Dort stimulieren sie das Zellwachstum und verhindern den Zelltod. „Wir haben einen optimalen Ladungsbereich gefunden, so dass das Molekül am Gewebe bindet, sich aber auch ablösen und nach innen diffundieren kann“, berichtet Geiger. Er hält weitere Einsatzgebiete für denkbar.
Den Knochen stabilisieren
Bei Osteoporose und einigen Krebsarten verlieren Knochen ihre Fähigkeit zur Regeneration. Sie werden spröde und brechen leicht. Aus Tierexperimenten ist bekannt, dass spezielle Wachstumsfaktoren die Knochenbildung aktivieren. Sie gelangen aber nur schwer an ihren Wirkort und werden schnell wieder abgebaut. Dendrimere könnten den Transport erleichtern und für höhere Wirkstoffkonzentrationen sorgen.
Dendrimere in der Krebstherapie
Damit nicht genug. Bereits vor rund einem Jahr zeigten Forscher des Royal Institute of Technology in Stockholm, dass sich Dendrimere auch zur Behandlung von Tumorerkrankungen eignen. Sie synthetisierten baumartige Molekülstrukturen mit Schwefelverbindungen und testeten ihr Therapieprinzip an Zellkulturen. Dendrimere hafteten sich an Krebszellen und wurden anschließend abgebaut. Dabei entstanden Sauerstoffradikale, und die Krebszellen gingen zugrunde.
Übertragbarkeit auf Patienten ist zu klären
In allen Fällen handelt es sich um Prof-of-Concept-Studien. Die Übertragbarkeit auf Menschen ist noch unklar. Viele Forscher rechnen jedoch bald mit klinischen Studien. Was die Sache einfacher macht: Ausgangsverbindungen der Dendrimere wie PEG sind gut charakterisiert, und toxische Effekte gelten als unwahrscheinlich.
Mehr zum Thema „Nanotechnologie“ unter:
Ein Beitrag von: