Coronaviren knipsen Recycling in Zellen aus
Mehr und mehr Patienten erkranken am neuartigen Coronavirus. Doch Therapien oder Impfungen gibt es nicht. Ein körpereigener Recycling-Mechanismus beim verwandten MERS könnte zur Achillesferse der Krankheit werden.
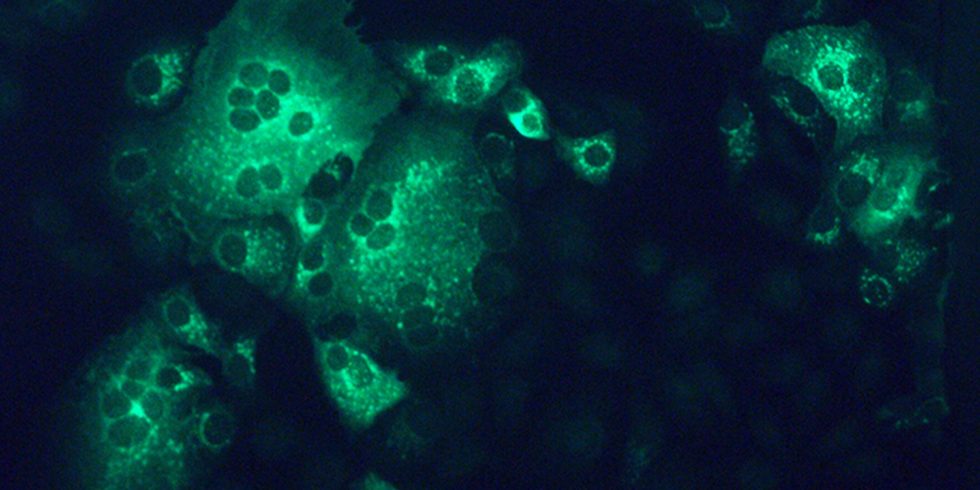
Affennierenzellen, die mit MERS-Coronaviren (grün) infiziert sind.
Foto: Müller/Charité
Rund 40.500 Infizierte, 910 Tote und etwa 3.500 Menschen mit erfolgreicher Genesung, so lautet die Bilanz zum neuen Coronavirus 2019-nCoV (10. Februar, 15:00 Uhr). Zwar sinkt die Zahl an Neuerkrankungen in China langsam. Gleichzeitig treten mehr Fälle in der EU (14 in Deutschland, 11 in Frankreich) auf. Japan (26), Australien (15), die USA (12) und Kanada (7) sind ebenfalls betroffen. Ein Ende der Infektionswelle zeichnet sich noch lange nicht ab.
Jetzt stehen Forscher vor großen Herausforderungen. Impfungen oder wirksame Arzneimittel fehlen. Deshalb verfolgen sie zwei Strategien. Sie arbeiten mit biologisch eng verwandten Erregern, etwa dem MERS-CoV (Middle East respiratory syndrome coronavirus). Und sie setzen, um Zeit zu sparen, bereits zugelassene Arzneistoffe ein. Das könnte im besten Fall Zeit bei klinischen Studien im Anschluss sparen. Zelluläre Recycling-Systeme erweisen sich als interessante Zielstruktur, berichten Forscher jetzt.
MERS bremst das zelluläre Recycling
Zum Hintergrund: Seit dem Jahr 2010 untersuchen Forscher das MERS-Coronavirus. Es führt – ähnlich wie 2019-nCoV – zu einer schweren Lungenentzündung, allerdings häufiger mit tödlichem Ausgang. Wissenschaftler des Deutschen Zentrums für Infektionsforschung (DZIF) an der Charité – Universitätsmedizin Berlin brachten in Erfahrung, dass MERS-Viren den zellulären Prozess der Autophagie herunterfahren. Erst dann gelingt es ihnen, Zellen zu infizieren.
Unter Autophagie versteht man einen Recycling-Mechanismus, den Zellen benötigen, um beschädigtes Material und Abfallprodukte abzubauen. Daraus entstehen Aminosäuren, Zucker oder Nukleinsäuren (Bausteine des Erbguts), um neue Moleküle herzustellen. Das spart biochemische Energie, verglichen mit dem kompletten Abbau zu Kohlendioxid und Wasser. Und die Synthese gelingt schneller.
Viren fallen der Autophagie ebenfalls zum Opfer. Sie werden in kleine, inaktive Einheiten zerschnitten. Doch die Erreger haben Strategien entwickelt, um sich dagegen zu wehren. Tatsächlich verlangsamt MERS in Zellen nach einer Infektion das biochemische Recycling. „Dieses Ergebnis war ein deutlicher Hinweis darauf, dass der MERS-Erreger von einer Abschwächung des zellulären Recyclings profitiert“, erklärt Marcel Müller vom Institut für Virologie am Campus Charité Mitte.
Ein Schalter für die Therapie von morgen
Im nächsten Schritt wollten die Forscher wissen, wie Zellen ihre Recycling-Maschinerie steuern. Sie fanden ein Eiweiß mit der Abkürzung SKP2 (S-phase kinase-associated protein 2) als entscheidende Struktur. MERS-Viren legen diesen molekularen Schalter um, und die Recycling-Einheit arbeitet nur noch auf Sparflamme. Das bedeutet: Viren entgehen dem biochemischen Schredder. Sie können weitere Zellen infizieren und sich im Organismus verbreiten. Die Krankheit schreitet voran.
Damit wird SKP2 zu einer interessanten Zielstruktur für die Behandlung viraler Infektionen. Sollte es gelingen, den Schalter so zu manipulieren, dass MERS ihn nicht mehr umlegen kann, hätten Viren schlechtere Karten bei Infektionen. Sie würden vielmehr abgebaut.
Gesagt, getan. Damit sich Viren nicht am Schalter SKP2 zu schaffen machen, inaktivierten Forscher dieses Eiweiß chemisch mit Hemmstoffen. Funktionierte SKP2 nicht mehr richtig, hatte MERS keine Möglichkeit mehr, die Autophagie zu verringern. Die Rechnung ging auf: Wirkstoffe verringerten die Virale Vermehrung stark, teilweise sogar um den Faktor 28.000. Unter den getesteten Substanzen befand sich auch ein bereits zugelassenes Molekül, nämlich Niclosamid. Ärzte verordnen es bei Bandwurmerkrankungen. Die Substanz gilt als vergleichsweise gut verträglich.
„Unsere Ergebnisse zeigen, dass SKP2 ein vielversprechender Ansatzpunkt für die Entwicklung neuer Wirkstoffe gegen das MERS-Virus – und möglicherweise auch gegen andere Autophagie-abhängige Viren – ist“, kommentiert Müller.
Klinische Studien erforderlich
„Für den Einsatz von SKP2-Hemmern als Medikamente fehlen allerdings noch Tests im Organismus“, ergänzt der Forscher. „Außerdem ist eine klare Risiko-Nutzen-Abwägung nötig, da auch bereits zugelassene Medikamente Nebenwirkungen haben können.“ Da MERS und das gerade zirkulierende Coronavirus 2019-nCoV biologische eng verwandt sind, könnte der neue Mechanismus vielleicht auch hier zu Therapiemöglichkeiten führen.
Das wird zuerst in präklinischen Studien an Versuchstieren getestet. Dann folgen klinische Studien mit gesunden Menschen, sprich Probanden, und mit Patienten. Das Prinzip soll mögliche Risiken minimieren. Zu Niclosamid gibt es jedoch schon viele Daten, was eine weitere Untersuchung beschleunigen könnte.
Mehr zum neuartigen Coronavirus
Ein Beitrag von: