Wie mRNA-Impfstoffe gegen COVID-19 das Immunsystem nachhaltig beeinflussen
Forschende der Universität zu Köln haben in einer neuen Studie gezeigt, dass mRNA-COVID-19-Impfstoffe das angeborene Immunsystem auf lange Sicht verändern.
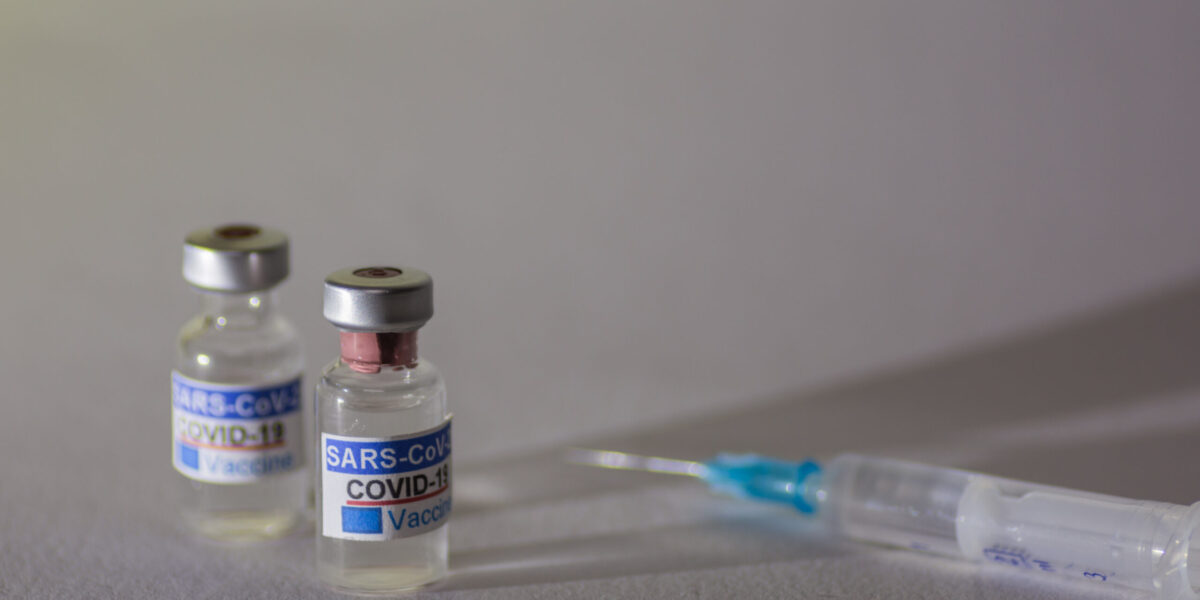
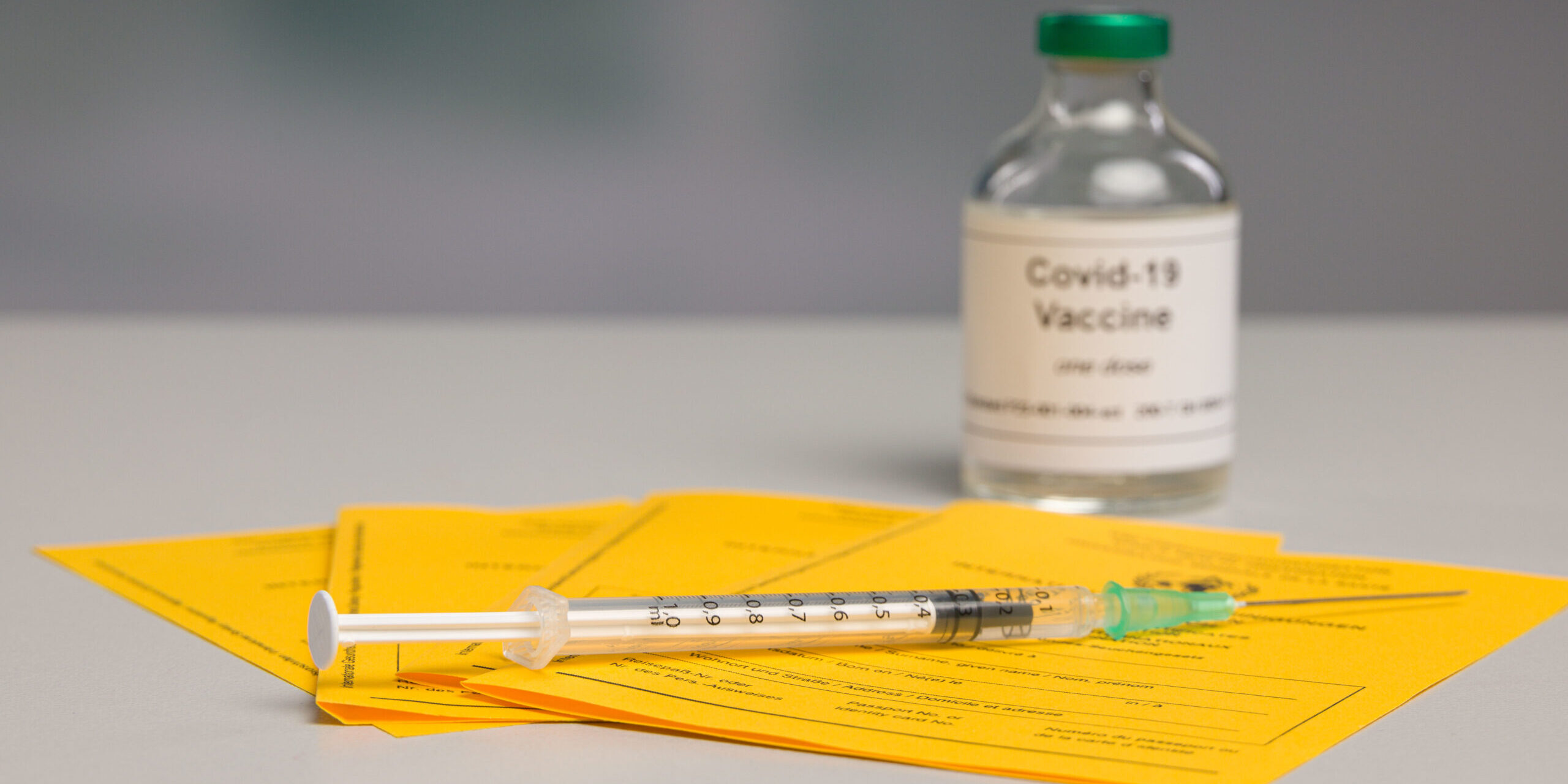
mRNA-Impfstoffe gegen COVID-19 verändern die Immunabwehr auf lange Sicht.
Foto: PantherMedia / thomas eder
Diese Veränderung kann dazu führen, dass der Körper bei zukünftigen Infektionen schneller und umfassender reagiert. Die Ergebnisse wurden in der Zeitschrift „Molecular Systems Biology“ veröffentlicht.
Die mRNA-Impfstoffe gegen COVID-19 lösen nicht nur die üblichen Immunantworten des adaptiven Immunsystems wie die Produktion von Antikörpern aus, sondern verursachen auch dauerhafte Veränderungen in den Abwehrzellen des angeborenen Immunsystems. Das zeigt eine Impfstudie von Forschern der Universität zu Köln und der Uniklinik Köln. Die Studie wurde von Professor Dr. Dr. med. Jan Rybniker und Dr. Robert Hänsel-Hertsch geleitet und im Fachjournal „Molecular Systems Biology“ veröffentlicht.
Das Immunsystem besteht aus zwei Teilen: dem angeborenen und dem adaptiven Immunsystem. Das angeborene Immunsystem bietet schnellen, unspezifischen Schutz vor Krankheitserregern, während das adaptive Immunsystem sich an neue oder veränderte Erreger anpasst. Beide Systeme arbeiten eng zusammen. In der aktuellen Studie fanden die Forschenden heraus, dass Veränderungen im angeborenen Immunsystem durch epigenetische Markierungen im Erbgut entstehen. „Epigenetisch“ bedeutet, dass Histone – Proteine, um die die DNA gewickelt ist – chemisch verändert werden können, ohne die DNA-Sequenz zu verändern. Diese Veränderungen könnten dazu führen, dass der Körper bei zukünftigen Infektionen schneller und umfassender reagiert.
Epigenetischen Veränderungen für eine langfristige Immunität
„Die Daten zeigen, dass mRNA-Impfstoffe eine epigenetische ‚Schulung‘ des angeborenen Immunsystems fördern, was eine verstärkte Immunantwort zu Folge hat“, erklärt Erstautor Dr. Alexander Simonis. Diese epigenetischen Veränderungen könnten eine langfristige und starke Immunität schaffen, die über den bekannten Schutz des erworbenen Immunsystems hinausgeht. Auf Basis der Studienergebnisse kann dies nun in größeren klinischen Studien weiter untersucht werden.
Die Wissenschaftler*innen untersuchten in Blutproben von geimpften Probanden zu sechs verschiedenen Zeitpunkten menschliche Monozyten – eine Art weißer Blutkörperchen, die sich im Körper zu Makrophagen entwickeln. Makrophagen gehören zum angeborenen Immunsystem und sind wichtig, um Krankheitserreger schnell zu erkennen und zu bekämpfen. Sie fanden heraus, dass die mRNA-Coronaimpfung eine deutliche und langanhaltende Veränderung durch Acetylierung verursacht, bei der eine chemische Gruppe an bestimmte Gene in den Monozyten bindet, die für die Immunabwehr wichtig sind.
Ein langfristiges „Gedächtnis“ des Immunsystems
Die Studie zeigte zudem, dass diese epigenetischen Veränderungen bis zu sechs Monate nach der Impfung erhalten blieben, was auf ein langfristiges „Gedächtnis“ des Immunsystems hinweist. Da Monozyten nur etwa drei Tage leben, vermutet das Team, dass auch die Vorläuferzellen der Monozyten im Knochenmark diese epigenetischen Markierungen haben.
„Erst eine zweite Impfung oder eine einzelne Auffrischungsimpfung – also eine Verstärkung der Immunisierung – stabilisierte die epigenetische Modifikation nachhaltig. Das unterstreicht die Notwendigkeit mehrerer Impfungen für die langfristige Aufrechterhaltung der Immunantwort“, erklärt Jan Rybniker.
Schutz vor anderen Viren und Bakterien?
Die beobachteten epigenetischen Veränderungen führten zu einer verstärkten Aktivierung entzündungsfördernder Gene, was die Produktion von Botenstoffen anregte, die zahlreiche Immunzellen aktivieren und deren Fähigkeit zur Bekämpfung von Infektionen verbessern können. Dr. Sebastian Theobald, einer der Erstautoren der Studie, erklärte, dass die Aktivierung des angeborenen Immunsystems, das relativ breit und unspezifisch auf verschiedene Erreger reagiert, darauf hindeutet, dass mRNA-Impfungen zumindest für eine gewisse Zeit auch Schutz vor anderen Viren und Bakterien bieten könnten.
Der Epigenetikexperte Dr. Robert Hänsel-Hertsch deutete darauf hin, dass diese Histon-Markierungen in Makrophagen nicht nur Gene aktivieren, die für die Immunantwort relevant sind, sondern dass diese Gene auch guaninreiche viersträngige DNA-Strukturen bilden, die für die langfristige Immunität von entscheidender Bedeutung sein könnten.
Ein Beitrag von: